CoronaVac: Anvisa aprova uso emergencial de mais 4,8 milhões de doses
O novo lote teve matéria-prima produzida na China, mas foram envasados no Instituto Butantan
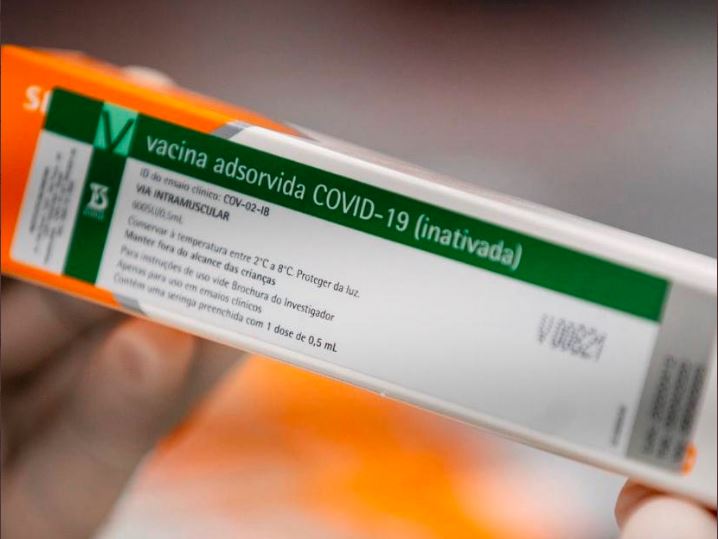
Agência Nacional de Vigilância Sanitária (Anvisa) aprovou o uso emergencial do segundo lote com 4,8 milhões de doses da vacina CoronaVac, contra a Covid-19, desenvolvida pelo laboratório Sinovac Biotec em parceria com o Instituto Butantan. O parecer favorável ocorreu após voto unânime dos diretores Meiruze Sousa Freitas, Romison Rodrigues Mota, Alex Machado Campos, Cristiane Rose Jourdan Gomes e do diretor-presidente Antônio Barra Torres.
Trata-se da segunda aprovação do antígeno pela agência. A diferença entre o primeiro e o segundo lote diz respeito à fabricação desas doses: as 6 milhões iniciais foram totalmente produzidas na China. As atuais têm matéria-prima produzida na China, mas foram finalizadas e envasadas no Instituto Butantan. Para conceder a autorização, a Anvisa comparou as duas produções para verificar se as aplicações têm as mesmas propriedades.
No entendimento da agência, o frasco multidoses —com dez aplicações — deve ser totalmente utilizado, uma vez aberto, em até 8 horas. Do contrário, a agência teme não garantir a integridade do antígeno. Na aprovação anterior não havia essa preocupação pois cada frasco continha apenas uma aplicação. A gerência-geral de medicamentos e produtos biológicos foi a primeira a sugerir a aprovação desse segundo lote.
LEIA TAMBÉM: Covid-19 em 2021: 4 certezas e 7 dilemas para o segundo ano da pandemia
O departamento de inspeção e fiscalização de insumos farmacêuticos apontou que nenhuma das 5.000 unidades de testes apresentaram contaminação pós-incubação, o que significa que o controle de qualidade cumpre seus requisitos no tema. Além disso, tanto a Sinovac quanto o Butantan têm pareceres positivos em inspeções de suas dependências de produção pela Anvisa. A Gerência-Geral de Inspeção e Fiscalização Sanitária também ratificou a recomendação estendendo-a a outros lotes produzidos da mesma maneira.
A diretora Meiruze Sousa Freitas relembrou a importância de que se cumpra o que está assinado no termo de compromisso assinado após a primeira aprovação de uso emergencial do medicamento . Esse documento determina que, até 28 de fevereiro, seja feita e apresentada à Anvisa a complementação dos estudos de imunogenicidade, conforme aprovado no desenho de estudo clínico fase III da vacina.
Também foi ressaltado que o Butantan deve enviar periodicamente resultados de estabilidade — algo como validade do medicamento — ao longo do tempo.
Confira o número de brasileiros já vacinados com as primeiras 6 milhões de doses da CoronaVac:
Nesta sexta-feira, 22, o Brasil teve médias móveis de 51. 489,7 casos confirmados e 999,6 mortes em decorrência da Covid-19.

 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO

 Tom pastoral de Marcos Mion destoa da crítica de Madonna no palco
Tom pastoral de Marcos Mion destoa da crítica de Madonna no palco Temer é consultado sobre manobra que livraria Bolsonaro de eventual prisão
Temer é consultado sobre manobra que livraria Bolsonaro de eventual prisão Madonna esconde rótulo de cerveja, joga garrafa e patrocinador vira meme
Madonna esconde rótulo de cerveja, joga garrafa e patrocinador vira meme Madonna: participação ‘muda’ de Anitta teve motivo prévio
Madonna: participação ‘muda’ de Anitta teve motivo prévio A razão de William Bonner usar avião da FAB para ir ao Rio Grande do Sul
A razão de William Bonner usar avião da FAB para ir ao Rio Grande do Sul







