Pfizer e Moderna testam novas estratégias de vacinação contra variantes
As empresas avaliam formas de aumentar a proteção de seus imunizantes contra as novas cepas do coronavírus
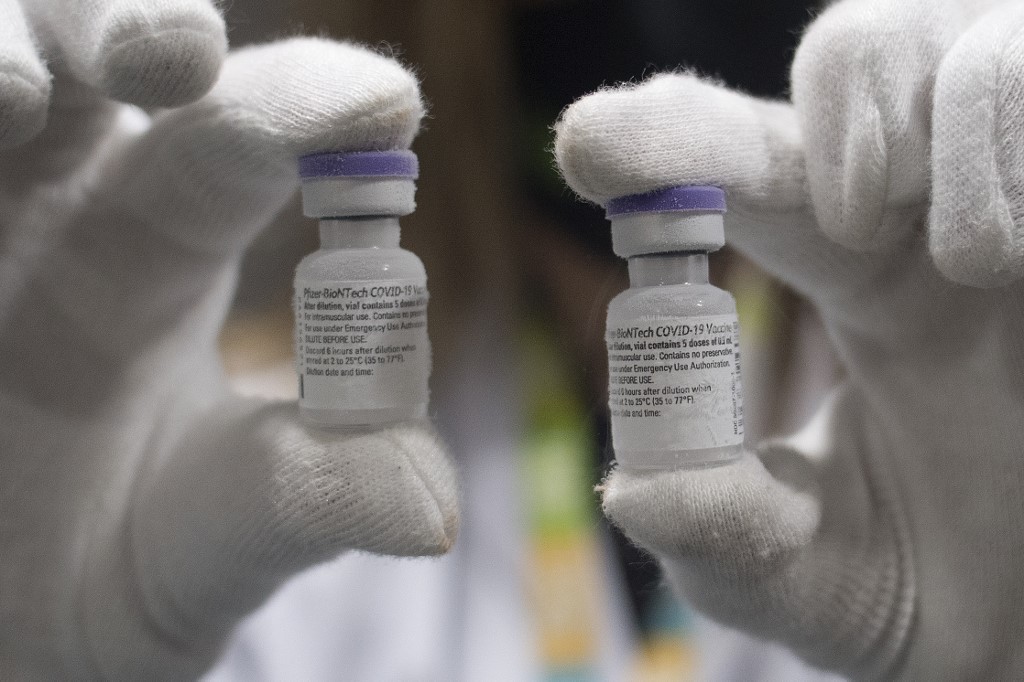
As novas variantes do coronavírus, em especial a B.1.351, identificada na África do Sul, preocupam especialistas e autoridades de saúde devido à sua possível resistência às vacinas contra Covid-19 disponíveis atualmente. Diante disso, algumas empresas buscam se antecipar e avaliar novas estratégias vacinais para aumentar a proteção contra as novas cepas.
Nesta quinta-feira, 25, a Pfizer e a BioNTech anunciaram um novo teste clínico que irá avaliar se a administração de uma terceira dose da vacina melhora a resposta imunológica contra as novas variantes. No estudo, até 144 voluntários que participaram da fase 1 de testes da vacina nos Estados Unidos receberão uma terceira dose do imunizante, administrada de 6 a 12 meses após as doses anteriores. O grupo incluirá alguns participantes idosos com até 85 anos de idade.
Os pesquisadores buscam avaliar a segurança e a resposta imunológica gerada por essa dose de reforço, além de entender quão bem esses anticorpos conseguirão neutralizar novas cepas em testes em laboratório. “Este estudo de reforço é crítico para compreender a segurança de uma terceira dose e eficácia contra cepas circulantes”, disse o CEO da Pfizer, Dr. Albert Bourla, em comunicado.
LEIA TAMBÉM: Suplementos de vitamina C e zinco não reduzem sintomas do coronavírus
As empresas também estão em discussão com autoridades regulatórias sobre a possibilidade de testar uma nova versão da vacina, modificada para proteger contra as novas variantes. No entanto, A Pfizer e a BioNTech ainda não veem evidências convincentes de que as variantes são resistentes à vacina atual.
Na quarta-feira, 24, a empresa americana Moderna, cuja vacina também utiliza a plataforma de mRNA, disse que produziu uma versão atualizada do imunizante contra a Covid-19 para a variante B.1.351. As doses iniciais dessa nova versão foram enviadas para os Institutos Nacionais de Saúde dos Estados Unidos (NIH, na sigla em inglês) para um estudo clínico.
A nova versão, chamada mRNA-1273.351, será avaliada de duas formas: como uma dose de reforço para pessoas que já foram vacinadas com a versão original e como uma vacina primária para pessoas que não tiveram Covid-19 e ainda não foram imunizadas.
A Moderna disse ainda que vai avaliar uma injeção de reforço “multivalente”, que combina a nova formulação da vacina com a original, e que começou a testar se uma terceira dose da vacina original, em concentração mais baixa, é capaz de aumentar a imunidade contra as novas variantes. A vacina atual requer duas doses de 100 microgramas com intervalo de cerca de um mês entre elas. As doses de reforço têm até metade deste nível.
“A Moderna está empenhada em fazer quantas atualizações forem necessárias em nossa vacina até que a pandemia esteja sob controle.”, disse Stephane Bancel, CEO da Moderna, em comunicado.
A empresa não informou em quanto tempo espera os resultados destes estudos ou quando a nova versão da vacina estará disponível para uso. Na segunda-feira, 22, a FDA, agência que regula medicamentos nos EUA, anunciou novas diretrizes que podem agilizar a liberação de novas versões de vacinas já aprovadas.
Testes em laboratório mostraram que a vacina da Moderna e da Vacina Pfizer têm eficácia reduzida contra a cepa sul-afriacana. Entretanto, ainda não se sabe se isso significa que pessoas que receberam os imunizantes estão menos protegidas contra a nova variante.

 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO


 Galvão Bueno tem contas penhoradas por dívida milionária de vinícola
Galvão Bueno tem contas penhoradas por dívida milionária de vinícola Shopping se manifesta sobre ‘calote’ de Taís Araújo
Shopping se manifesta sobre ‘calote’ de Taís Araújo Mais um dia na vida de Elon Musk: ações da Tesla caem, carros encalham
Mais um dia na vida de Elon Musk: ações da Tesla caem, carros encalham A milionária conta dos carros blindados de Eduardo Paes no Rio
A milionária conta dos carros blindados de Eduardo Paes no Rio Interpol atende Argentina e emite alerta de prisão contra ministro do Irã
Interpol atende Argentina e emite alerta de prisão contra ministro do Irã







