Covid-19: Anvisa autoriza uso emergencial da vacina da Janssen
Antígeno de dose única tem 38 milhões de doses garantidas ao Brasil, mas aplicações só devem chegar no último trimestre do ano
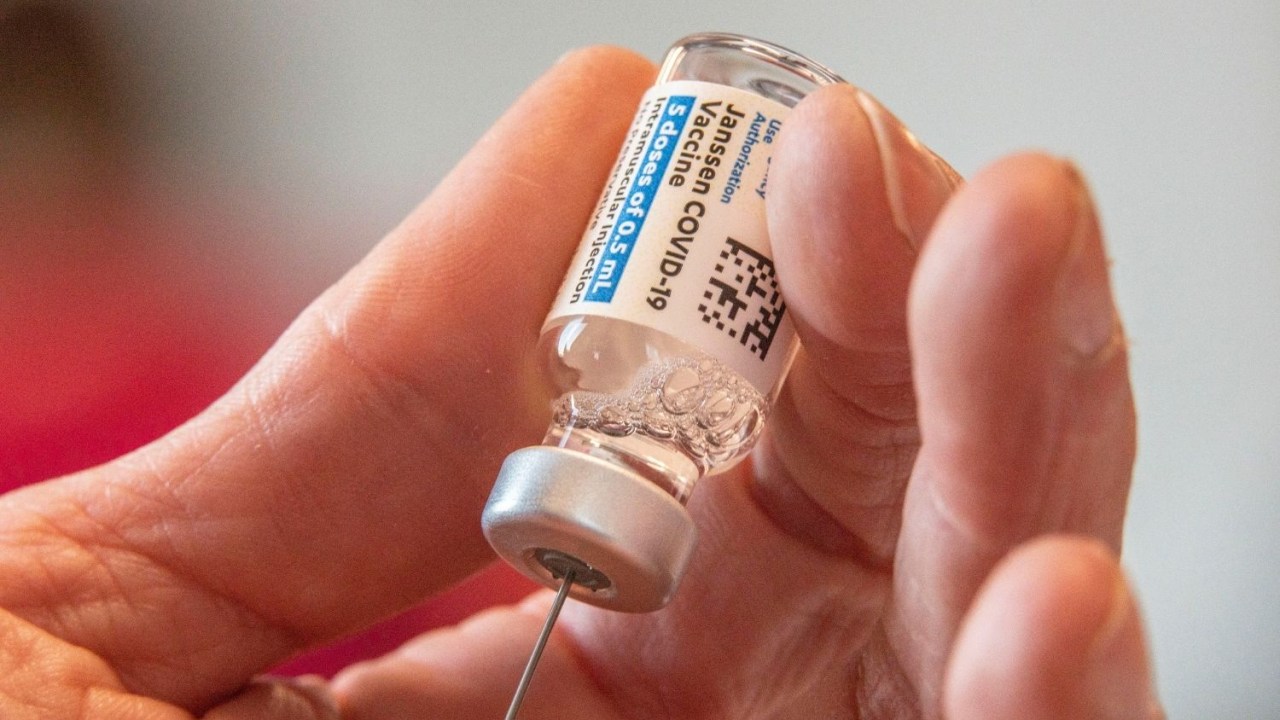
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou nesta quarta-feira, 31, o uso emergencial da vacina da Janssen, braço farmacêutico da Johnson & Johnson. Trata-se do terceiro antígeno a receber tal liberação temporária no Brasil. A vacina da Pfizer não passou por essa etapa e recebeu diretamente a autorização total.
O imunizante — único que permite a proteção com apenas uma dose — tem 38 milhões de doses garantidas pelo Ministério da Saúde, mas todas as entregas devem ocorrer somente no último trimestre deste ano.
Votaram positivamente à liberação os diretores da Anvisa Meiruze Sousa Freitas, Rômison Rodrigues Mota e Alex Machado Campos — que formaram a maioria simples necessária para o aval.
LEIA TAMBÉM: Vacina da Johnson & Johnson contra Covid-19: as vantagens e desvantagens
O antígeno foi estudado no Brasil, com a participação de 7.500 voluntários. No mundo, foram por volta de 40.000 de pessoas a receberem as agulhadas do imunizante ou de um medicamento placebo. Nessas análises, foi identificado que a vacina é efetiva para indivíduos com idades superior a 18 anos com e sem comorbidades, incluindo idosos. Além disso, o fármaco foi caracterizado como seguro para uso da população.
Outros estudos confirmatórios, porém, ainda precisam ser realizados em grupos específicos — como o das gestantes. Há também atenção prioritária à efetividade da vacina diante de variantes da Covid-19. O gerente-geral de Medicamentos, Gustavo Mendes afirmou que essas informações adicionais relacionadas à mutações ainda não foram enviadas à agência.
De acordo com documentos exibidos pela Anvisa, a resposta imune começa a ocorrer 14 dias após a primeira — e única — aplicação. A eficácia global foi de 66,9%. A vacina já é aprovada emergencialmente em países como Estados Unidos, Suíça, Estados Unidos e pela agência de controle da União Europeia.

 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO


 Galvão Bueno tem contas penhoradas por dívida milionária de vinícola
Galvão Bueno tem contas penhoradas por dívida milionária de vinícola Shopping se manifesta sobre ‘calote’ de Taís Araújo
Shopping se manifesta sobre ‘calote’ de Taís Araújo Mais um dia na vida de Elon Musk: ações da Tesla caem, carros encalham
Mais um dia na vida de Elon Musk: ações da Tesla caem, carros encalham A milionária conta dos carros blindados de Eduardo Paes no Rio
A milionária conta dos carros blindados de Eduardo Paes no Rio Interpol atende Argentina e emite alerta de prisão contra ministro do Irã
Interpol atende Argentina e emite alerta de prisão contra ministro do Irã







