Anvisa recebe pedido de uso emergencial da vacina do Butantan
Agência diz que já iniciou a triagem dos documentos presentes na solicitação; meta é fazer a análise do uso emergencial em até 10 dias
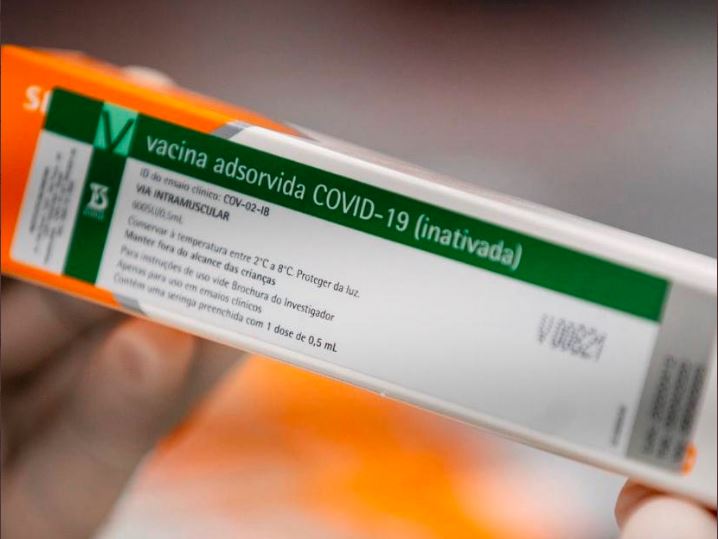
A Anvisa acaba de receber nesta sexta o pedido de autorização temporária de uso emergencial, em caráter experimental, da vacina CoronaVac.
O pedido foi enviado pelo Instituto Butantan, que no Brasil conduz os estudos da vacina desenvolvida pela chinesa Sinovac.
A Anvisa já iniciou a triagem dos documentos presentes na solicitação e da proposta de uso emergencial que o laboratório pretende fazer.
As primeiras 24 horas, segundo a agência, serão utilizadas para fazer uma triagem do processo e checar se todos os documentos necessários estão disponíveis. Se houver informação importante faltando, a Anvisa pode pausar o prazo e solicitar as informações adicionais ao laboratório.
Para fazer sua avaliação, a Anvisa vai utilizar as informações apresentadas junto com o pedido e também as informações já analisadas pela Anvisa por meio da submissão contínua. A análise do pedido de uso emergencial é feita por uma equipe multidisciplinar, envolve especialista das áreas de registro, monitoramento e inspeção. A equipe vem atuando de forma integrada, com as ações otimizadas e acompanhadas pela comissão que envolve três diretorias da agência.
A meta da Anvisa é fazer a análise do uso emergencial em até 10 dias, descontando eventual tempo que o processo possa ficar pendente de informações a serem apresentadas pelo laboratório.
Por fim, a Anvisa atua, conforme os procedimentos científicos e regulatórios, os quais devem ser seguidos por aqueles que buscam o a autorização de vacinas para serem utilizadas na população brasileira.


 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO


 Cenários da Globo estão na mira da Justiça: uso indevido de tecnologia
Cenários da Globo estão na mira da Justiça: uso indevido de tecnologia Com decisões equivocadas, governo Lula aumenta a incerteza na economia
Com decisões equivocadas, governo Lula aumenta a incerteza na economia As ameaças de viúva de Gal Costa à namorada de herdeiro
As ameaças de viúva de Gal Costa à namorada de herdeiro O motivo para TV Globo desistir da exibição do Festival de Parintins
O motivo para TV Globo desistir da exibição do Festival de Parintins A mudança drástica na trama de Bridgerton para incluir personagem lésbica
A mudança drástica na trama de Bridgerton para incluir personagem lésbica







