Gilead aumenta 50 vezes capacidade de produção do remdesivir
A farmacêutica prometeu entregar 12,5 milhões de doses do tratamento até o final do ano
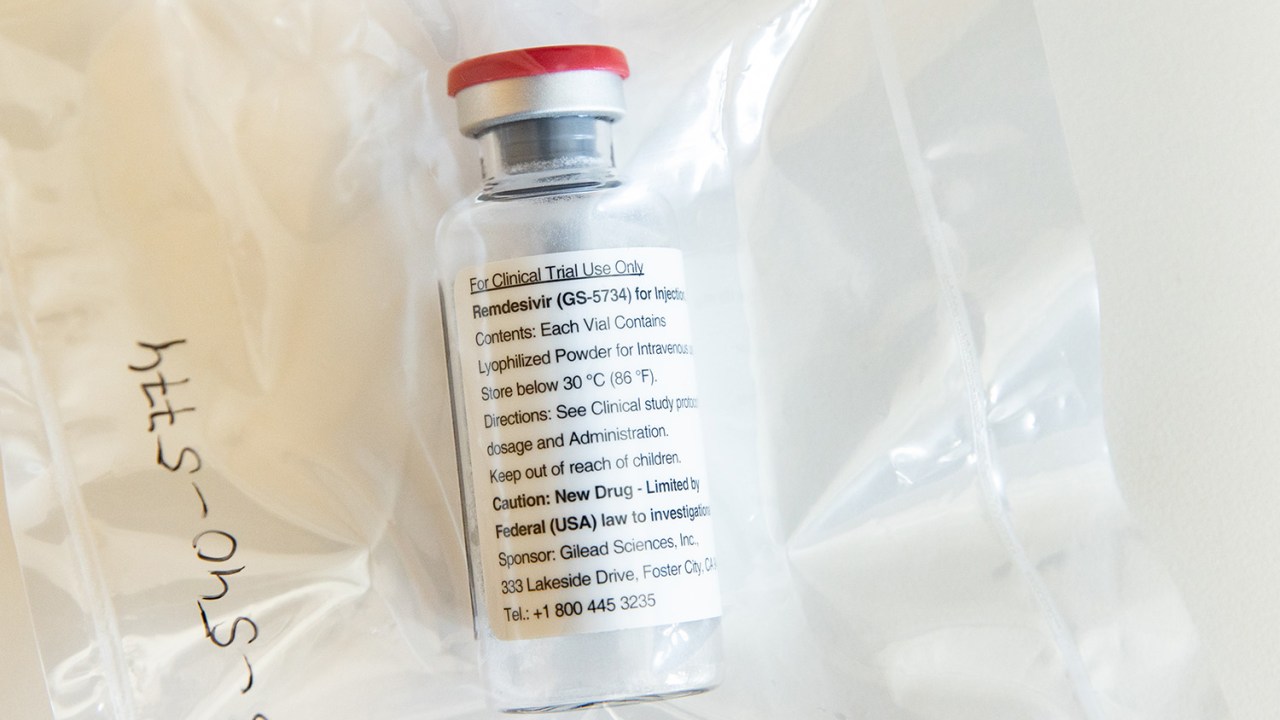
A farmacêutica americana Gilead Sciences Inc aumentou em 50 vezes sua capacidade de produção do antiviral remdesivir desde janeiro. De acordo com a empresa, a partir de outubro será possível atender em tempo real a demanda global. O medicamento é o único aprovado até o momento para o tratamento do coronavírus nos Estados Unidos e na Europa.
“Aumentamos a oferta em mais de 50 vezes desde janeiro e prevemos poder atender a demanda global em tempo real a partir de outubro. Planejamos produzir mais de dois milhões de cursos de tratamento até o final do ano e prevemos produzir vários milhões a mais em 2021, se necessário.”, disse a Gilead em comunicado. Os dois milhões de cursos de tratamento equivalem a 12,5 milhões de doses.
Além de melhorias no processo, que conseguiram reduzir o tempo de fabricação para seis meses, a empresa precisou expandir a rede global de fábricas, com a realização de parcerias. A Gilead firmou acordos de licenciamento voluntário com nove fabricantes de genéricos em todo o mundo, o que permitirá expandir a oferta do remdesivir para 127 países, a maioria de baixa e média-baixa renda.
LEIA TAMBÉM: “Não conhecemos os efeitos do uso indiscriminado da ivermectina”
A notícia significa um alívio para os países que temiam ficar sem acesso ao medicamento, após os Estados Unidos terem comprado praticamente todo o estoque da droga. Originalmente, o remdesivir foi desenvolvido para tratar ebola. Entretanto, sua eficácia deixou a desejar nos testes clínicos e ele nunca foi aprovado. Surpreendentemente, o medicamento demonstrou capacidade de combater o novo coronavírus ao interferir em sua capacidade de replicação.
O remdesivir está na vanguarda da luta contra o novo coronavírus desde que a droga ajudou a reduzir o tempo de recuperação hospitalar em um ensaio clínico com pacientes graves. Por outro lado, o tratamento não foi capaz de melhorar a sobrevida dos pacientes após duas semanas de acompanhamento. Os resultados de um estudo com quatro semanas de acompanhamento são esperados em breve


 Premiê ucraniano diz que haverá Terceira Guerra Mundial se Rússia vencer
Premiê ucraniano diz que haverá Terceira Guerra Mundial se Rússia vencer A mais longa das noites: países árabes cooperaram com Israel contra Irã
A mais longa das noites: países árabes cooperaram com Israel contra Irã O curioso elogio a Wagner Moura em ‘Guerra Civil’, segundo americanos
O curioso elogio a Wagner Moura em ‘Guerra Civil’, segundo americanos Filho de Renata Lo Prete diz como se inspira nos horários notívagos da mãe
Filho de Renata Lo Prete diz como se inspira nos horários notívagos da mãe Pesquisa revela o tamanho do prejuízo em bares e restaurantes no RJ
Pesquisa revela o tamanho do prejuízo em bares e restaurantes no RJ







