Análise criteriosa descartou ligação de morte com Coronavac, diz HC/USP
Segundo Esper Kallás, coordenador dos testes, hospital informou a Anvisa e seguiu todas as regras éticas de pesquisa no episódio envolvendo um voluntário
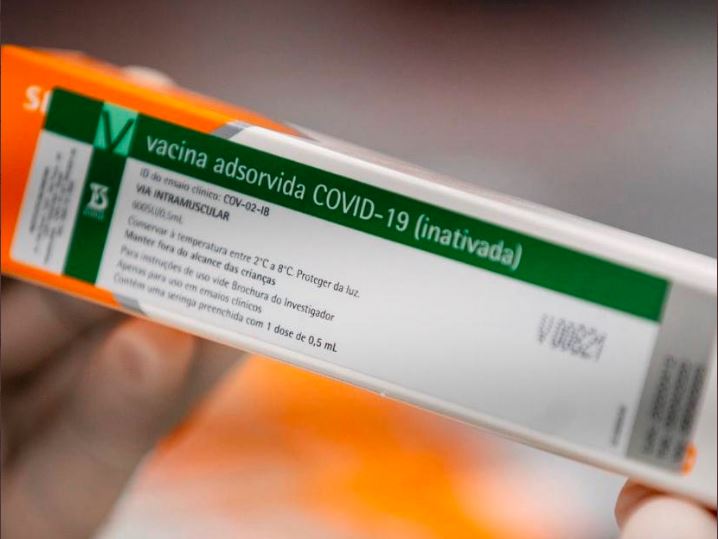
O infectologista Esper Kallás, coordenador dos testes envolvendo a vacina Coronavac no Hospital das Clínicas da Universidade de São Paulo (USP), afirmou, em carta divulgada na tarde desta terça-feira, 10, que o “evento adverso grave” que levou a Anvisa (Agência Nacional de Vigilância Sanitária) a suspender os testes com o imunizante produzido pelo Instituto Butantan e a farmacêutica chinesa Sinovac não teve relação nenhuma com o teste.
O evento adverso ao qual se referiu a Anvisa foi a morte de um voluntário que estava participando da fase 3 do estudo no HC, que é vinculado à Faculdade de Medicina da USP. “A equipe de investigadores, em análises criteriosas sobre o ocorrido, concluiu que o evento não está relacionado à vacina em teste”, disse Kallás.
A morte do voluntário foi decorrência de suicídio, de acordo com laudo emitido pelo Instituto Médico Legal (IML) de São Paulo.
Segundo Kallás, o evento foi notificado à Comissão Nacional de Ética em Pesquisa (Conep) e à Anvisa “nos prazos regulatórios estipulados por ambos”. “O HC FMUSP está em contato permanente com o Butantan, Conep e Anvisa para esclarecer todos os fatos sobre o ocorrido”, afirmou.
Ele também afirmou que o HC/USP “reitera seu mais profundo respeito à afirmação no documento de suspensão” emitido pela Anvisa de que “os dados sobre voluntários de pesquisas clínicas devem ser mantidos em sigilo, em conformidade com princípios de confidencialidade, dignidade humana e proteção dos participantes.”
“O HC/FMUSP sempre irá realizar todas as pesquisas clínicas em pleno respeito às normas de Boas Práticas de Pesquisa Clínica e Declaração de Helsinki, da qual o Brasil é signatário”, afirmou.
Butantan
Sem dar detalhes do que aconteceu com o voluntário por sigilo médico, o diretor do Butantan, Dimas Covas, declarou que era “impossível” a causa do óbito ter qualquer relação com a aplicação da vacina. “Nós estamos tratando aqui de um evento adverso grave que não tem relação com a vacina. Essa informação está disponível na Anvisa desde o dia 6, quando foi notificado o evento adverso grave”, afirmou Covas em entrevista coletiva realizada no Instituto Butantan. “Os estudos deverão ser retomados em dois dias”, disse ele.




 Justiça procura por Rafa Kalimann para pagar dívida à Perdigão
Justiça procura por Rafa Kalimann para pagar dívida à Perdigão Parceria de C&A e Globo gera chiadeira de atrizes poderosas da TV
Parceria de C&A e Globo gera chiadeira de atrizes poderosas da TV A adolescente franzina que criou um problemão para os árbitros da ginástica
A adolescente franzina que criou um problemão para os árbitros da ginástica O impacto bilionário do Brasil com estudantes de medicina no exterior
O impacto bilionário do Brasil com estudantes de medicina no exterior A cena de ‘Renascer’ que promete embrulhar o estômago do telespectador
A cena de ‘Renascer’ que promete embrulhar o estômago do telespectador









