
Em 1994, cinco anos depois de ter encerrado seus dois mandatos como presidente dos Estados Unidos, o republicano Ronald Reagan (1911-2004) escreveu uma carta aberta à população: “Soube recentemente que sou um dos milhões de americanos acometidos pela doença de Alzheimer”. Naquela época, pessoas com o mesmo diagnóstico de Reagan tinham apenas um único medicamento aprovado pelas autoridades para tratamento do mal que promove a degradação inevitável da memória e da cognição, o tacrina. De lá para cá, houve fenomenais avanços para a compreensão da dramática enfermidade, mas pouco, muito pouco, se andou na direção de novos medicamentos. Na segunda-feira 7, contudo, deu-se um estrondoso anúncio, celebrado por pacientes e familiares: a FDA, a agência americana reguladora de remédios, deu aval para o uso de uma droga que promete retardar a evolução do quadro em estágios iniciais. É o primeiro tratamento para Alzheimer, que acomete 45 milhões de pessoas no mundo, sendo 1,2 milhão no Brasil, aprovado nos últimos dezoito anos.
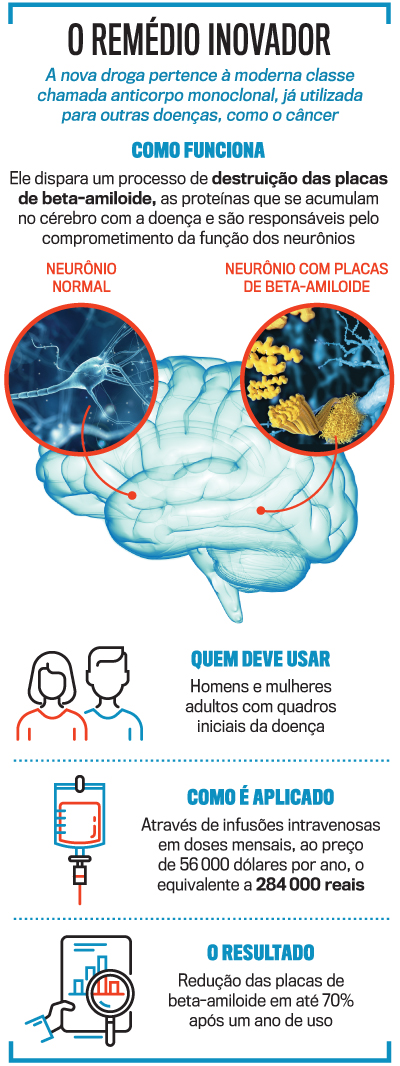
Desenvolvido pela empresa de biotecnologia americana Biogen em parceria com a farmacêutica Eisai, do Japão, o aducanumabe, eis o nome da substância, age no mecanismo causador do problema. Em testes, o fármaco foi capaz de romper as chamadas placas de beta-amiloides, formadas por um tipo de proteína que se acumula próximo aos neurônios e causam seu comprometimento e morte (veja no quadro abaixo). A presença desses aglomerados são, em geral, marcadores decisivos para a existência do Alzheimer no paciente, que passa a apresentar sintomas característicos, como dificuldade em pensar e compreender, falha na memória e permanente falta de concentração. “Trata-se de um passo de imensa relevância, atalho para uma série de novos estudos”, diz Victor Calil, neurologista e pesquisador do Instituto D’Or. “Mas é preciso, ainda, cautela para que se decrete a descoberta da terapia definitiva para o Alzheimer.”
Não é, de fato, a bala de prata. Mas há otimismo e celebração diante de um problema cercado de enigmas. Os usuários que participaram dos estudos com o aducanumabe conseguiram manter atividades rotineiras como fazer compras, alimentar-se, ir ao banco e tomar banho. A FDA, no entanto, pediu testes complementares em meio à intensa guerra interna. No ano passado, aliás, uma comissão de especialistas independentes recomendou adiar o sim definitivo para o produto. Novas rodadas de investigações, contudo, fizeram a locomotiva andar. “Um remédio com tais características pode ser estudado, no futuro, até mesmo como forma de prevenção para pessoas com alto risco de desenvolver a doença”, diz Daniel Ciampi, neurologista do Hospital Sírio-Libanês, em São Paulo. Em breve, ele poderá ser usado no Brasil. Os fabricantes já entraram com pedido de aprovação junto à Anvisa. “É comum os pacientes de Alzheimer e familiares perguntarem sobre novos medicamentos ou testes de diagnóstico”, diz a psiquiatra Tânia Ferraz Alves, diretora das enfermarias do Instituto de Psiquiatria da Universidade de São Paulo. É ansiedade justificável para uma enfermidade delicada e doída. Nas palavras da protagonista vivida por Julianne Moore em Para Sempre Alice: “Temos a sensação de não estar nem cá nem lá, como um personagem numa terra bizarra. É um lugar muito solitário e frustrante para se estar”.
Publicado em VEJA de 16 de junho de 2021, edição nº 2742


 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO





 O passado criminoso de um dos maiores campeões da música pop dos anos 80
O passado criminoso de um dos maiores campeões da música pop dos anos 80 As dívidas do homem que explodiu bombas na frente do STF
As dívidas do homem que explodiu bombas na frente do STF Banco rebaixa classificação do Brasil e aumenta aposta na Argentina
Banco rebaixa classificação do Brasil e aumenta aposta na Argentina A Geração Z está trocando o Spotify por uma tecnologia retrô
A Geração Z está trocando o Spotify por uma tecnologia retrô A data mais esperada pelos fãs de novelas entediados com ‘Mania de Você’
A data mais esperada pelos fãs de novelas entediados com ‘Mania de Você’








