A aposta no remdesivir, antiviral com ótimos resultados contra a Covid-19
Os primeiros estudos internacionais com o remédio dão sinais fortes rumo a um tratamento eficaz da infecção pelo novo coronavírus
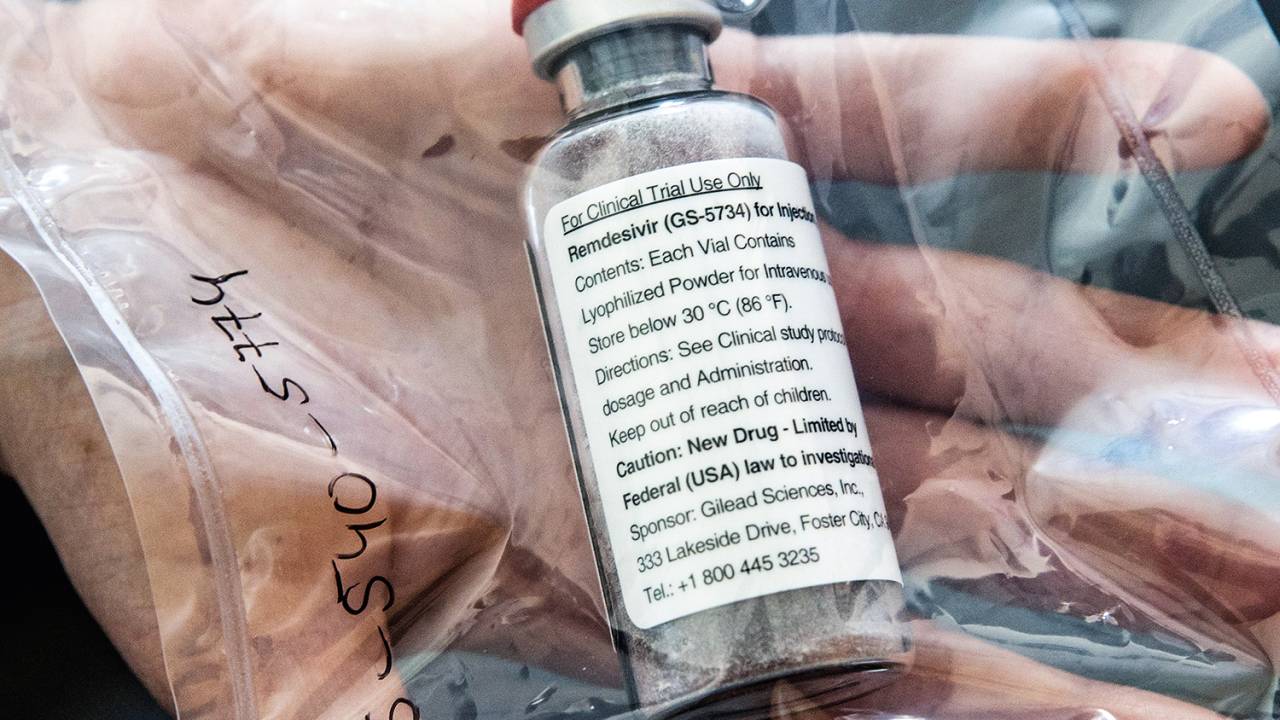
Lá no outro mundo em que vivíamos, em fevereiro, quando a Covid-19 começava a se espalhar, ainda silenciosa e sorrateiramente, o consultor sênior da Organização Mundial da Saúde (OMS), o canadense Bruce Aylward, alocado na China, mal foi escutado ao chamar atenção para um composto químico desenvolvido em um laboratório da farmacêutica Gilead, em Foster City, na Califórnia, ao sul de São Francisco. “Há apenas uma droga com real eficácia contra a Covid-19”, disse Aylward. “É o remdesivir.” Criado em laboratório há exatos oito anos — o primeiro estudo foi publicado na revista Bioorganic & Medicinal Chemistry Letters em 15 de abril de 2012 —, o antiviral foi aplicado em dois outros momentos. Inicialmente, nas pesquisas em torno de um possível tratamento do surto de Mers, a síndrome respiratória por coronavírus, identificada na Arábia Saudita, naquele mesmo ano do primeiro registro científico do medicamento. E, depois, como terapia em casos africanos de ebola, na Guiné, Serra Leoa e Libéria, entre 2013 e 2016. Nos episódios da Mers, verificou-se em laboratório uma freada na multiplicação do vírus. Com o ebola, houve testes em humanos, mas os resultados foram decepcionantes.

A segunda vida do remdesivir, celebrada agora nos corredores da OMS, veio à luz de forma quase anedótica, bem ao modo de nosso tempo, o das redes sociais, da internet. No dia 16, o conteúdo de um vídeo sobre um estudo da Universidade de Chicago com 125 doentes (113 deles com infecções graves) foi vazado pela Stat News, uma influente publicação americana do setor de saúde. Nele, Kathleen Mullane, especialista em doenças infecciosas e líder dos ensaios clínicos, informava que, depois de iniciado o tratamento com o remdesivir, os pacientes tiveram a febre diminuída rapidamente e alguns saíram dos ventiladores no dia seguinte. “Mas a melhor notícia é que a maioria dos nossos voluntários se recuperou e apenas dois morreram”, ela afirmou. A resposta pôde ser rapidamente medida em dólares. Pouco mais de quinze minutos após a celebração de Kathleen, as ações da Gilead, a fabricante da droga, saltaram até 14% nas bolsas de Chicago e Nova York. O índice financeiro Stoxx 600, que reúne pequenas e médias empresas de países europeus, registrou ganhos de 2,9%. O FTSE, de Londres, subiu 3,2%. Deu-se alguma oscilação natural nos dias seguintes, mas a Gilead cresceu e apareceu — e, tudo indica, definitivamente.
As curvas ascendentes dos papéis foram o eco financeiro, medida de interesse global, atrelado a um par de ótimas notícias. Além dos dados vazados, outro trabalho, cujas conclusões foram publicadas na reputada revista científica The New England Journal of Medicine (NEJM), apontou boas respostas com o remdesivir. Um grupo de 53 pacientes afetados pela Covid-19 recebeu por via intravenosa 200 miligramas do antiviral e, na sequência, foi tratado ao longo de nove dias com 100 miligramas da substância. Depois de dezoito dias, 68% dos doentes apresentaram melhora na condição clínica — entre os trinta casos mais graves, controlados por meio de ventilação mecânica, na UTI, dezessete pacientes deixaram o quarto de tratamento intensivo. Do grupo inicial, sete pessoas morreram. Parece muito, mas o medicamento foi ministrado quando a situação já era desesperadora, e, mesmo assim, mais da metade se recuperou.

O renascimento do remdesivir, que anima os mercados e representa uma esperança, muito além de uma quimera, é a tradução de um dos movimentos mais fascinantes da aventura histórica da medicina, em especial da epidemiologia: substâncias originalmente desenvolvidas para determinada enfermidade são aplicadas, com sucesso, em outra. A trajetória mais espetacular foi de outro antiviral, a zidovudina, mais conhecida pela sigla AZT, que se mostraria eficaz no combate ao vírus HIV, da aids. Desenvolvida em 1964 como fármaco contra a leucemia, foi deixada de lado depois do desempenho ruim em testes com ratos. O criador da medicação, o americano Jerome Horwitz (1919-2012), guardou as anotações numa gaveta e disse a seus colegas da Wayne State University, em Detroit, uma frase que se tornaria célebre: “Desenvolvemos um conjunto muito interessante de compostos que aguardam a doença certa”. A partir da eclosão da aids, a inesperada e triste “doença certa”, o AZT voltou a entrar na engrenagem dos laboratórios. Foi patenteado pela farmacêutica Burroughs Wellcome (Horwitz nada recebeu) e, em 1987, quase 25 anos depois dos passos iniciais, acabou aprovado oficialmente pela rigorosa FDA, a agência de controle de saúde dos Estados Unidos. Em São Francisco, com o anúncio, foram organizados bailes de rua pela comunidade de homossexuais, então o grupo de risco mais atingido pela síndrome, para celebrar a boa-nova, o prólogo de um coquetel que salvaria vidas. A bioquímica Janet Rideout, agora com 81 anos, envolvida na descoberta da relação do AZT com o HIV, lembra-se daqueles dias como quem esteve na frente de batalha de uma guerra, e a metáfora ainda hoje é pertinente. “Trabalhávamos em altíssima velocidade”, recorda. “Havia muito nervosismo quando chegava a hora de administrar o medicamento aos pacientes pela primeira vez. Era assustador pensar que poderíamos prejudicar as pessoas que queríamos socorrer.”
A velocidade que se impunha é a mesma que se exige atualmente — e, tanto para o AZT quanto para o remdesivir, a corrida autorizou e autoriza a supressão de algumas etapas, como ocorre com a criação de uma vacina (veja a reportagem na pág. 54). O motivo é simples: não há tempo a perder. A conduta é atrelada a riscos. Os próprios cientistas da fabricante Gilead admitem algumas fragilidades, ainda, embora tenham a anuência das autoridades de saúde para seguir em frente. As investigações divulgadas na semana passada foram ancoradas em uma metodologia conhecida como “teste aberto”, em que médicos e pacientes sabiam que o remdesivir estava sendo ministrado — o padrão acatado hoje é o “duplo-cego”, em que ambas as partes trabalham com desconhecimento sobre o remédio oferecido. Evidências estatísticas realmente válidas virão de levantamentos mais amplos. Nesses ensaios, os doentes são divididos aleatoriamente em dois grupos — um recebe remdesivir e o outro, placebo.

Um estudo mais detalhado, dentro dos rigorosos moldes exigidos pela boa medicina, está sendo conduzido pela universidade americana de Nebraska. Iniciado em meados de fevereiro, terá os primeiros resultados concluídos em três semanas. Trata-se da pesquisa com o mais curto tempo para aprovação das autoridades do governo na história dos Estados Unidos. Financiada pelos Institutos Nacionais da Saúde (NIH) americanos, ela investiga a ação do remdesivir em 500 infectados de setenta instituições de saúde de diversos países, acometidos pela doença, em estado clínico de média e alta gravidade. “Estou esperançoso, mas o ímpeto para a descoberta da bala de prata não pode comprometer a ciência séria”, disse a VEJA o infectologista e intensivista brasileiro André Kalil, um dos coordenadores do trabalho de Nebraska.
Na terça-feira 21, autoridades dos NIH informaram, claramente, a inexistência de remédios já aprovados para o controle da Covid-19 — mas puseram o remdesivir no grupo de substâncias que aguardam “dados definitivos de ensaios clínicos para identificar tratamentos ideais”. Faz parte do pacote outro antiviral, a famosa cloroquina, a droga da ideologia, desenhada originalmente contra malária, lúpus e artrite reumatoide. Cabe aqui fazer uma pergunta que não quer calar: por que, afinal de contas, apostar no remdesivir e não na cloroquina? “Os primeiros relatos que indicam a eficácia da cloroquina, um antiviral e anti-inflamatório disponível no mercado e barato, contra uma epidemia desconhecida nos entusiasmaram”, afirma a pesquisadora da molécula Ludhmila Hajjar, intensivista do Instituto do Coração (Incor), em São Paulo. “Mas o tempo tem mostrado que os resultados não representaram melhora real para os doentes.” Entre os problemas estão efeitos colaterais drásticos, como arritmia e defeitos visuais. Há relatos de mortes em decorrência das aplicações. São obstáculos que não foram identificados na trajetória do remdesivir com a Mers e o ebola, apesar da insuficiência de certezas. Ressalte-se, ainda, que o remdesivir atua de modo muito mais direto no controle da circulação do coronavírus no organismo (veja o quadro na pág. 50).

Não seria exagero dizer, portanto, que estamos hoje, com três décadas de avanços em tecnologia e ciência, em momento semelhante ao da véspera do bater de tambores com o AZT — talvez seja cedo ainda, talvez haja demasiado e humano otimismo, mas dados os investimentos em jogo (só nos Estados Unidos, despendem-se 8 bilhões de dólares, o equivalente a 44 bilhões de reais, em pesquisas com o remdesivir e similares) e o empenho da OMS, além da iniciativa privada, há uma avenida aberta, como a de uma cidade em isolamento. A disputa, paralela e positiva, é outra — o que virá antes, um medicamento poderoso, sem falsas promessas, como pode ser o remdesivir, associado a mecanismos de fortalecimento do sistema imunológico (veja o quadro na pág. 52), ou a vacina. É uma luminosa luta pela vida.
Publicado em VEJA de 29 de abril de 2020, edição nº 2684


 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO

 A falta que faz o Ensino Superior aos maiores influenciadores do Brasil
A falta que faz o Ensino Superior aos maiores influenciadores do Brasil Ator e produtor se casam rodeados de famosos; confira fotos
Ator e produtor se casam rodeados de famosos; confira fotos A estreia de Fafá de Belém no TSE da ministra Cármen Lúcia
A estreia de Fafá de Belém no TSE da ministra Cármen Lúcia As novas proibições da Anvisa para canetas antiobesidade importadas
As novas proibições da Anvisa para canetas antiobesidade importadas ‘Ele lutou contra a lei e a lei venceu’, diz ‘The Guardian’ às vésperas de prisão de Bolsonaro
‘Ele lutou contra a lei e a lei venceu’, diz ‘The Guardian’ às vésperas de prisão de Bolsonaro


















