Saiba como foi o segundo transplante de coração de porco em humano
Com uma doença cardíaca terminal, Lawrence Faucette é mais um xenotransplantado nos Estados Unidos
Em 2022, eram necessários mais de 40 mil transplantes de córnea, rim, fígado, coração e pulmão no Brasil. Ainda assim, somente cerca de 21 mil transplantes desses órgãos foram realmente feitos no ano passado. Todos os dias, pessoas morrem enquanto esperam um órgão novo, já que as doações são insuficientes para todos. No entanto, o xenotransplante – ou transferência de células, tecidos e órgãos entre espécies – pode ser uma alternativa para resolver essa escassez.
Nos anos 1960, pesquisadores experimentaram usar babuínos e chimpanzés como doadores de órgãos para seres humanos, com algum sucesso, mas as dificuldades em criá-los foram limitantes. Os porcos, ao contrário, são produzidos em larga escala pela agropecuária – além de ter órgãos com dimensões e anatomias próximas ao homem, esses animais podem ser criados em condições controladas e submetidos a testes mais demorados para estudos genéticos e pesquisa de agentes infecciosos, possibilidade que os doadores humanos não dispõem em virtude da urgência em transplantar o órgão antes que se torne inviável.
Nesse contexto, David Bennett, de 57 anos, foi o primeiro paciente a receber um coração de porco, em setembro de 2020. Bateu no peito do receptor durante oito longas semanas antes de parar, não por falha própria, mas como consequência de uma infecção por citomegalovírus, agente oportunista que se aproveita da imunossupressão associada aos transplantes. Apesar da sobrevida curta, o avanço foi enorme.
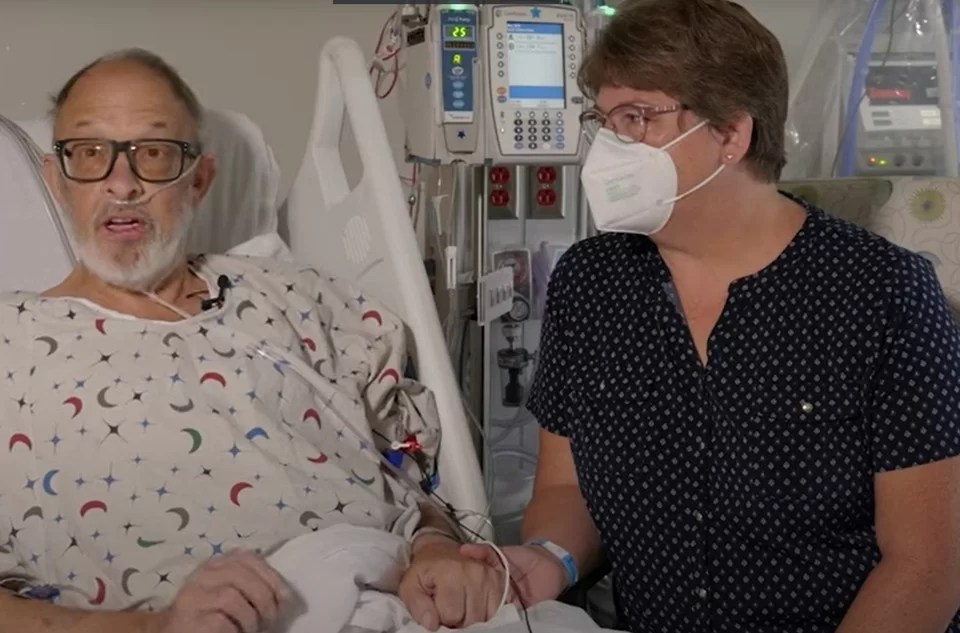
Agora, Lawrence Faucette, de 58 anos, com uma doença cardíaca em estágio terminal, se junta a Bennett como mais um xenotransplantado. De acordo com os médicos da Universidade de Maryland, nos Estados Unidos, que também realizaram a primeira intervenção, o paciente – 2ª pessoa no mundo a receber o transplante de um coração de porco geneticamente modificado, em setembro – já respira sozinho e o coração funciona bem, sem assistência de dispositivos de suporte.
“Minha única esperança real é o coração de porco. Pelo menos agora tenho uma chance”, disse Faucette, pai de dois filhos, à rede CNN. De fato, sua doença cardíaca estava em estágio terminal, o que o tornou inelegível para um transplante tradicional.
Ajuste genético
A maior pedra no sapato de qualquer transplante é a rejeição, quando o corpo não reconhece o órgão e, assim, tenta eliminá-lo, o que também pode acontecer em xenotransplantes. Um estudo lançado na ultima semana no periódico cientifico Lancet, por exemplo, relata que “apesar dos efeitos favoráveis a curto prazo e da ausência de lesões hiperagudas”, os casos sugerem que ainda é necessário avanços para melhorar essas questões no xenotransplante.
O resultado de 2020 chamou a atenção do mundo científico, porque órgãos ou células de outra espécie começam a ser rejeitados em minutos. Na comparação, dois meses são uma eternidade. Mas o desafio da rejeição hiperaguda permanece. Não se pode simplesmente aparecer na fazenda, escolher um porco, abatê-lo e transplantar seus órgãos. Por isso, até por volta de 2005, os cientistas se dedicaram a modificar geneticamente esses animais, antes mesmo de nascerem.
A edição genética envolve knockouts (bloqueios) e knock-ins (adições) de genes. Os recentes transplantes de rim e coração utilizaram órgãos dos “porcos de 10 genes”, especialmente projetados para essa função. Eles possuem um ajuste genético para evitar que seus órgãos doados reajam aos hormônios do crescimento humano e se expandam fora de controle.
Outra alteração importante remove uma molécula de açúcar, chamada alfa-Gal, que adere à superfície das células dos porcos e age como se fosse um luminoso de neon gigante, que marca o tecido como sendo totalmente externo. Um braço do nosso sistema imunológico, chamado sistema complementar, patrulha constantemente o corpo em busca de alfa-Gal. É por isso que os órgãos podem ser rejeitados e mortos momentos após o transplante e a célula modificada é introduzida em um óvulo sem núcleo (material genético), mesma técnica de transferência aprendida com a ovelha Dolly, mesmo não sendo uma clonagem.
Tentativa e erro
Apesar do déficit de órgãos ser uma urgência atual, o xenotransplante ainda não é a solução. “É um assunto em evolução”, afirma Fabio Biscegli Jatene, Diretor da Divisão de Cirurgia Cardiovascular e Vice-Presidente do Conselho Diretor do InCor. “O que se cria com esses primeiros casos é a perspectiva que é possível. A partir dai, é trabalhar para viabilizar o xenotransplante em larga escala.”
Jatene faz parte de um grupo de pesquisadores brasileiros que estuda o tema a fundo. Junto a ele, coordena o projeto Silvano Raia, o primeiro cirurgião na América Latina a realizar um transplante de fígado em 1985, e Mayana Zatz, bióloga molecular e geneticista brasileira.
Em resumo, o projeto brasileiro já consegue modelar a genética, “com o nascimento de porcos geneticamente modificados em alguns meses”, relata Jatene. Como o campo ainda é muito penumbre, há várias escolas de pensamento, principalmente quantos genes deverão ser adicionados ou retirados. No transplante americano, como dito, é o porco de dez genes alterados, já o estudo brasileiro escolhe retirar apenas três.
O grupo também trabalha na frente de perfusão isolada, com um suporte artificial de vida realizado por equipamentos que deixa um órgão funcionando fora do organismo por dias ou meses. Uma vez completada as duas etapas, a ideia é juntar uma a outra. Ou seja, ter órgãos geneticamente modificados funcionando fora de um corpo.
Como fica claro, o tema dos xenotransplantes ainda será alvo de intenso debate nos próximos anos ao redor do mundo, até que a prática se torne uma realidade para muita gente.



 Trump anuncia nova tarifa de 25% e leva disputa comercial para as estradas
Trump anuncia nova tarifa de 25% e leva disputa comercial para as estradas Por que Leão XIV decidiu reverter reforma imposta pelo papa Francisco
Por que Leão XIV decidiu reverter reforma imposta pelo papa Francisco Como Manuela Dias promoveu infantilização de Cauã Reymond e Alice Wegmann
Como Manuela Dias promoveu infantilização de Cauã Reymond e Alice Wegmann A resposta de Virginia após provocação de MC Poze envolvendo Vini Jr
A resposta de Virginia após provocação de MC Poze envolvendo Vini Jr Centrão pula fora do barco se Eduardo insistir com candidatura à Presidência
Centrão pula fora do barco se Eduardo insistir com candidatura à Presidência




