Remdesivir, aprovado por agência americana, é testado em humanos no Brasil
Medicamento é usado no tratamento do presidente americano Donald Trump e é classificado como um dos mais promissores no combate à doença
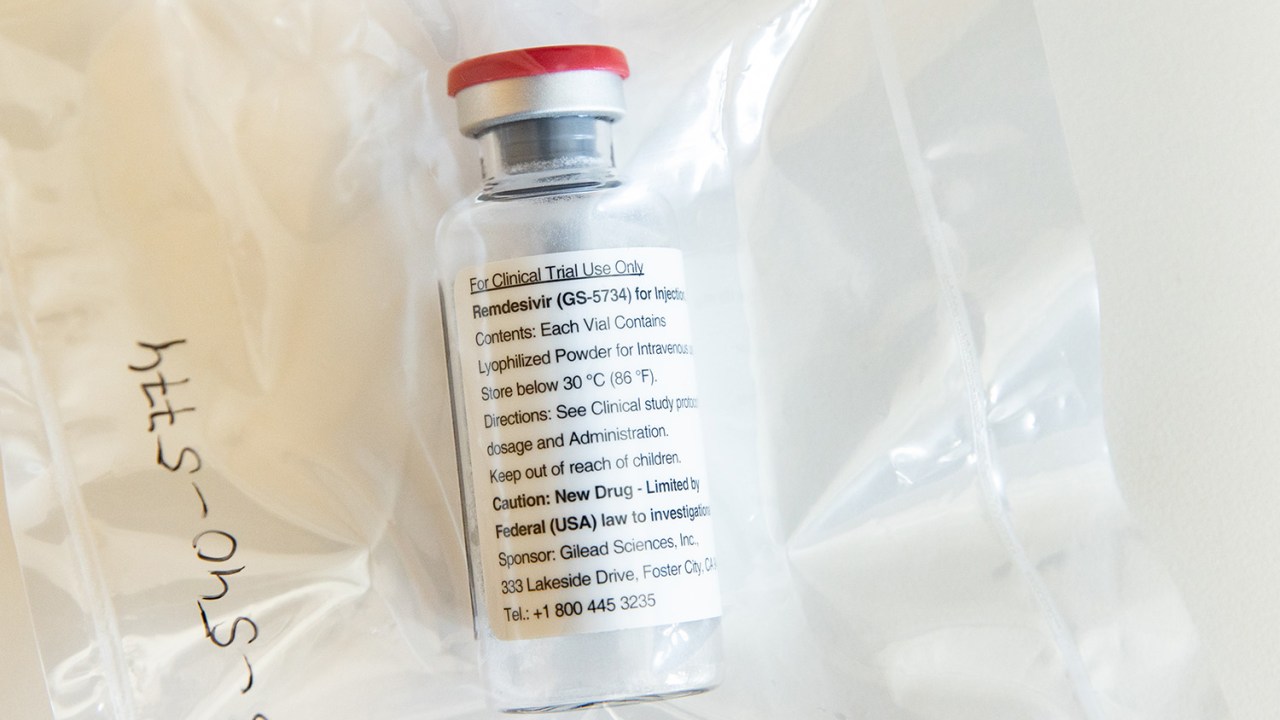
O antiviral Remdesivir, um dos remédios anunciados pela equipe médica da Casa Branca para o tratamento do presidente dos Estados Unidos, Donald Trump, diagnosticado com a Covid-19 na semana passada, é aprovado em caráter emergencial pela rigorosa agência de medicamentos americana FDA (do inglês Food and Drug Administration) para casos em adultos e crianças internados com a infecção ou quadros suspeitos nos EUA.
O Brasil entrou no cenário com dois estudos importantes de fase III, isto é, com a participação de voluntários humanos para testar o medicamento. Trata-se de um esforço de grande porte, com o envolvimento de diversas instituições brasileiras renomadas. O primeiro deles faz parte de um esforço internacional da Organização Mundial da Saúde (OMS) no projeto de nome “Solidariedade” em que há também a testagem de outros fármacos. O trabalho é coordenado no país pela Fundação Oswaldo Cruz (Fiocruz) e conta com importantes centros médicos a exemplo do Instituto de Infectologia Emilio Ribas e o Hospital Sírio-Libanês, ambos em São Paulo.
“São estudos que buscam apontar com assertividade a segurança e eficácia do Remdesivir o que já foi mostrado em estudos preliminares” diz Roberto Kalil, diretor-geral do centro de cardiologia do hospital Sírio-Libanês, em São Paulo. Participam das análises pacientes positivos para Covid-19 em quadros agravados ou moderados da doença, internados por pelo menos três dias. “Uma vez confirmada a eficácia do medicamento é esperado que a OMS o determine como um tipo de tratamento padrão”, diz a infectologista Mirian Dal Ben, também do Sírio-Libanês.
Outro estudo que também leva o Remdesivir em suas análise é coordenado pelo Instituto do Coração, em São Paulo. Ali, não se busca, no entanto, identificar a eficácia do Remdesivir, mas sim compreender sua reação combinada a um outro fármaco, o Tocilizumabe. Isso porque em alguns pacientes graves de Covid-19 a resposta imunológica do organismo é exagerada, podendo causar, entre outos efeitos, danos nos pulmões. A ideia é entender se o uso combinado dos dois medicamentos poderá, de alguma forma, atenuar este efeito. “Apesar de ser um mecanismo de defesa importante, em alguns pacientes é intensivo demais. Estamos tentando entender se é possível ocorrer o bloqueio da substância que causa a reação exagerada”, diz Lenio Alvarenga, diretor de Acesso e Médico da Roche Farma Brasil, responsável pelo medicamento utilizado em combinação.
Até agora 85 pacientes já tomaram o Remdesivir combinado com este fármaco — originalmente dedicado ao tratamento de atrite reumatoide — ou o Remdesivir com placebo. São sete centros participantes ao todo, entre eles a Faculdade de Medicina do ABC.
Estudos em laboratório
Na Unifesp, as análises com o Remdesivir ocorrem em laboratório, sem voluntários, mas sim com células infectadas. “Estamos estudando sua ação e seu mecanismo de funcionamento, assim podederemos determinar qual a melhor forma de utiliza-lo”, disse a VEJA, a reitora da instituição Soraya Smaili. A especialista em farmacologia, no entanto, alerta que estudos clínicos (ou seja, com a participação de pessoas) capntaneados pela universidade e por outras instituições de ensino seriam dificultados por conta do alto preço de importação do fármaco. Na Agência Nacional de Vigilância Sanitária (Anvisa) ainda não há pedido de registro (ou seja, a liberação comercial) do Remdesivir no Brasil.
Remdesivir
O remdesivir é um antiviral que atua bloqueando a replicação do vírus. Criado em laboratório há oito anos, inicialmente sua eficácia foi avaliada no combate ao surto de Mers, a síndrome respiratória por coronavírus, identificada na Arábia Saudita. Depois, foi usado como terapia em casos africanos de ebola, na Guiné, Serra Leoa e Libéria, entre 2013 e 2016. Nos episódios da Mers, verificou-se em laboratório uma freada na multiplicação do vírus. Com o ebola, o resultados de testes em humanos foram considerados decepcionantes.
O medicamento ganhou atenção ainda nos meses iniciais da pandemia ao apresentar resultados preliminares promissores no tratamento de pacientes graves com a Covid-19. Os estudos foram publicados no reputado New England Journal of Medicine. Em 1º de maio, a rigorosa agência reguladora de medicamentos dos Estados Unidos (FDA, do inglês Food and Drug Administration) autorizou o uso do fármaco antiviral em pessoas infectadas pelo novo coronavírus. A liberação emergencial, é importante dizer, não tem a mesma validade que uma aprovação formal do medicamento. Em abril, uma reportagem de capa de VEJA detalhou as pesquisas com o remédio.
Nesta quarta-feira, 7, o Brasil teve médias móveis atualizadas em 27.108,4 diagnósticos e 610,9 mortes por conta do novo coronavírus.

 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO


 Premiê ucraniano diz que haverá Terceira Guerra Mundial se Rússia vencer
Premiê ucraniano diz que haverá Terceira Guerra Mundial se Rússia vencer A mais longa das noites: países árabes cooperaram com Israel contra Irã
A mais longa das noites: países árabes cooperaram com Israel contra Irã Corrupção leva CNJ a avaliar plano de intervenção no Judiciário da Bahia
Corrupção leva CNJ a avaliar plano de intervenção no Judiciário da Bahia Filho de Renata Lo Prete diz como se inspira nos horários notívagos da mãe
Filho de Renata Lo Prete diz como se inspira nos horários notívagos da mãe Dívida de Taís Araújo em condomínio vira caso de Justiça
Dívida de Taís Araújo em condomínio vira caso de Justiça







