Agência europeia começa processo de análise da CoronaVac
Esse é o primeiro passo para um futura aprovação do imunizante no bloco, o que pode abrir caminho para a entrada de brasileiros
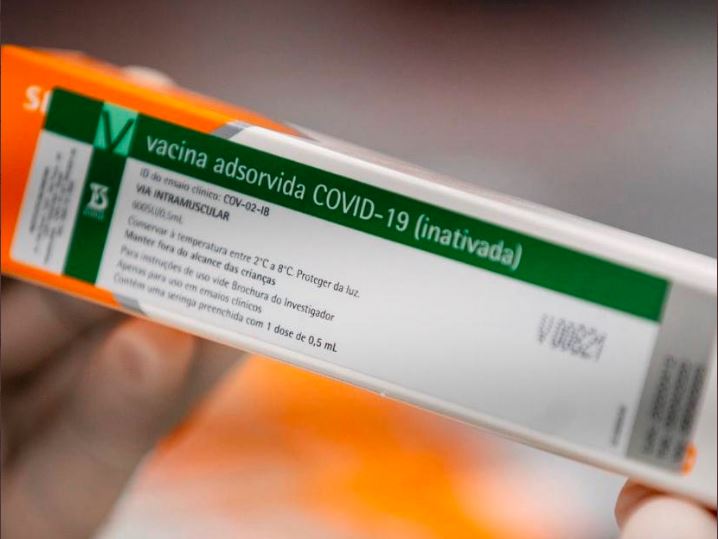
A EMA, agência que regula medicamentos na União Europeia, começou nesta terça-feira, 4, o processo de análise continuada da vacina contra Covid-19 desenvolvida pela empresa chinesa Sinovac Life Sciences. Esse é o primeiro passo para uma futura aprovação do imunizante no bloco.
“A revisão contínua continuará até que evidências suficientes estejam disponíveis para um pedido formal de autorização de comercialização.”, disse a EMA em comunicado. O Comitê de Medicamentos Humanos da EMA (CHMP, na sigla em inglês) irá avaliar se os benefícios da vacina superam os riscos e se sua eficácia, segurança e qualidade seguem os padrões exigidos pela União Europeia.
De acordo com a agência, a decisão de iniciar a revisão da vacina foi baseada em resultados de estudos laboratoriais e clínicos que sugerem que o imunizante, que na Europa é chamado Vero Cell e no Brasil, de CoronaVac, desencadeia a produção de anticorpos contra o novo coronavírus e pode ajudar a proteger contra a Covid-19.
LEIA TAMBÉM: Covid-19: por que é importante tomar a segunda dose da vacina
Atualmente, quatro vacinas contra a Covid-19 estão autorizadas no bloco: Pfizer-BioNTech, Moderna, AstraZeneca e Janssen. Todas passaram pelo processo de análise continuada.
Uma eventual aprovação da vacina da Sinovac na União Europeia pode facilitar a entrada de brasileiros no bloco. A Comissão Europeia pretende autorizar a entrada de viajantes provenientes de países que estejam com a pandemia controlada – o que não é o caso do Brasil no momento – ou que tiverem tomado duas doses de vacinas aprovadas na União Europeia ou pela Organização Mundial da Saúde (OMS).

 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO

 Shopping se manifesta sobre ‘calote’ de Taís Araújo
Shopping se manifesta sobre ‘calote’ de Taís Araújo Mais um dia na vida de Elon Musk: ações da Tesla caem, carros encalham
Mais um dia na vida de Elon Musk: ações da Tesla caem, carros encalham Eduardo Suplicy surpreende ao comparecer em aniversário de Mano Brown
Eduardo Suplicy surpreende ao comparecer em aniversário de Mano Brown Ivanir dos Santos entra com representação contra Ludmilla: ‘É crime’
Ivanir dos Santos entra com representação contra Ludmilla: ‘É crime’ A mais longa das noites: países árabes cooperaram com Israel contra Irã
A mais longa das noites: países árabes cooperaram com Israel contra Irã







