Agência europeia aceita pedido de registro da Sputnik V
Cabe à EMA determinar a velocidade de revisão das informações e decidir se autoriza o uso do imunizante no bloco
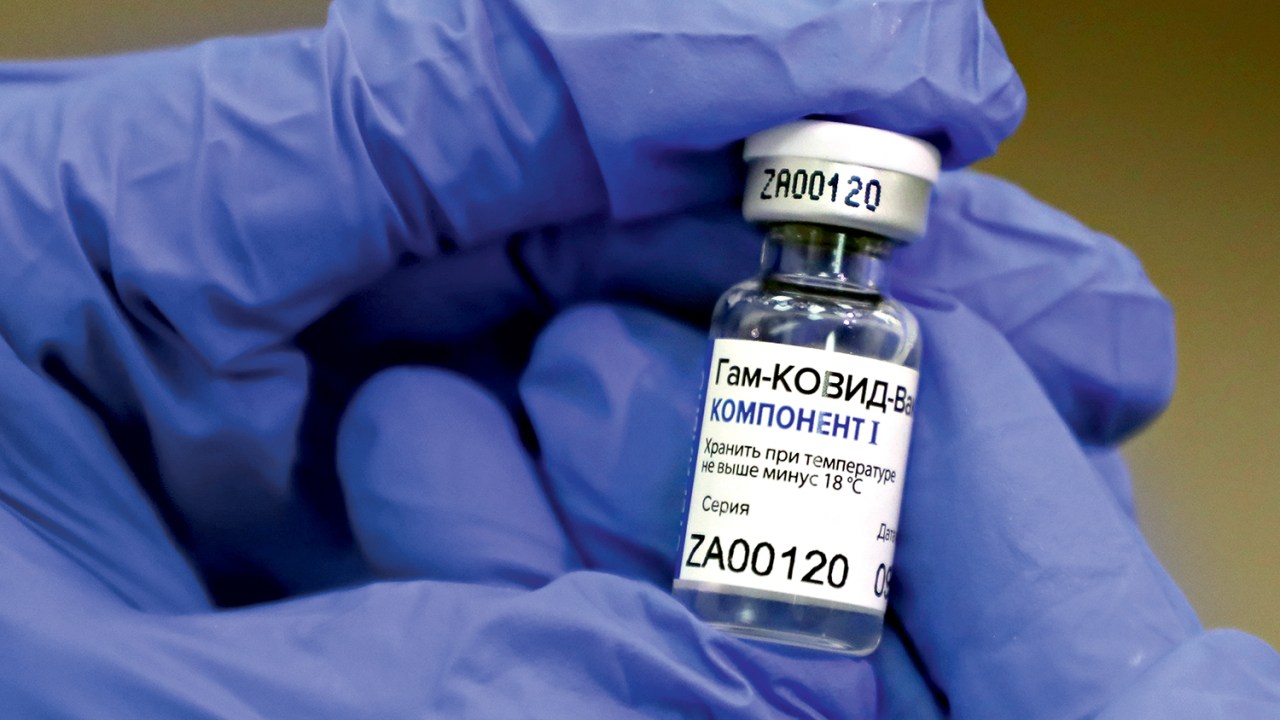
A EMA, agência que regula medicamentos na União Europeia, aceitou a submissão do pedido de registro da Sputnik V. Segundo informações do Fundo Russo de Investimento Direto (RDIF, na sigla em inglês), o processo de Revisão Científica da Sputnik V na EMA teve início em 22 de outubro do ano passado. Essa etapa foi realizada em 19 de janeiro. Dez dias depois, em 29 de janeiro, o Fundo enviou os documentos para solicitação do registro da vacina no bloco.
“O fundo tem uma confirmação oficial da EMA de que sua inscrição foi aceita.”, disse o RDIF, em comunicado nesta terça-feira, 9. Agora, cabe à agência á revisar as informações e decidir se autoriza o uso do imunizante no bloco. Ainda não há prazo para que isso aconteça.
A Sputnik V já teve seu uso autorizado em 17 países, mas ainda não passou pelo crivo de agências regulatórias tradicionais, como a americana, europeia, japonesa e britânica. No domingo, 7, a Hungria se tornou o primeiro membro da União Europeia a aprovar o uso emergencial da Sputnik V.
LEIA TAMBÉM: Vacina Sputnik V contra Covid-19: o que saber sobre eficácia e segurança
A decisão é uma tentativa de aumentar a disponibilidade de vacinas no país, após reclamar da lentidão da distribuição das vacinas por parte das autoridades do bloco europeu. Outros países, como França e Alemanha, já demonstraram interesse na vacina russa.
A União Europeia já autorizou o uso emergencial de três vacinas contra a Covid-19: Pfizer-BioNTech, Moderna e AstraZeneca.
No Brasil, a União Química, empresa responsável pela produção e distribuição do imunizante no país, já entrou com o pedido de aprovação da Anvisa, mas, segundo a agência, faltam documentos para dar início à revisão do processo. O Ministério da Saúde anunciou recentemente que negocia com o RDIF a compra inicial de 10 milhões de doses da vacina.
Na semana passada, um estudo publicado na revista científica The Lancet, comprovou a eficácia de 91,6% da vacina contra a Covid-19, o que aumentou o interesse no imunizante ao redor do mundo.

 SEGUIR
SEGUIR
 SEGUINDO
SEGUINDO

 Premiê ucraniano diz que haverá Terceira Guerra Mundial se Rússia vencer
Premiê ucraniano diz que haverá Terceira Guerra Mundial se Rússia vencer A mais longa das noites: países árabes cooperaram com Israel contra Irã
A mais longa das noites: países árabes cooperaram com Israel contra Irã Corrupção leva CNJ a avaliar plano de intervenção no Judiciário da Bahia
Corrupção leva CNJ a avaliar plano de intervenção no Judiciário da Bahia Filho de Renata Lo Prete diz como se inspira nos horários notívagos da mãe
Filho de Renata Lo Prete diz como se inspira nos horários notívagos da mãe Elon Musk: quando a liberdade de expressão encontra a fantasia
Elon Musk: quando a liberdade de expressão encontra a fantasia







